Причины, особенности и методы защиты от электрохимической коррозии
Причины, особенности и методы защиты от электрохимической коррозии
Среди всех существующих видов разрушения металлов наиболее часто встречается электрохимическая коррозия, которая возникает в результате его взаимодействия с электролитически проводящей средой. Основная причина данного явления – это термодинамическая неустойчивость металлов в средах, которые их окружают.

Этому виду коррозии подвержены многие объекты и конструкции:
- газовые и водные трубопроводы;
- элементы транспортных средств;
- другие конструкции, изготовленные из металла.
Коррозийные процессы, то есть, ржавчина, могут возникать в атмосфере, в грунте, и даже в соленой воде. Очистка металлоконструкций от проявлений электрохимической коррозии является сложным и длительным процессом, поэтому проще предотвратить ее возникновение.
Основные разновидности
При коррозии в электролитах происходит преобразование химической энергии в электрическую. В связи с этим ее называют электрохимической. Принято различать следующие виды электрохимической коррозии.
Межкристаллитная
Под межкристаллитной коррозией подразумевается такое опасное явление, при котором происходит разрушение границ зерна никеля, алюминия и других металлов избирательным образом. Как следствие, прочностные и пластичные свойства материала утрачиваются. Главная опасность этой разновидности коррозии в том, что далеко не всегда она заметна визуально.

Питтинговая
Питтинговая электрохимическая коррозия представляет собой точечное поражение отдельных участков поверхности меди и других металлов. В зависимости от характера поражения, различают закрытый, открытый, а также поверхностный питтинг. Размеры пораженных участков могут варьироваться от 0,1 мм до 1,5 мм.

Щелевая
Щелевой электрохимической коррозией принято называть усиленный процесс разрушения металлических конструкций в местах расположения щелей, зазоров и трещин. Протекание щелевой коррозии может происходить в воздушной атмосфере, газовых смесях, а также морской воде. Данный вид разрушения характерен для газопроводов, днищ морских судов и многих других объектов.
Распространено протекание коррозии в условиях небольшого количества окислителя из-за затрудненного подхода к стенкам щели. Это приводит к накоплению коррозийных продуктов внутри зазоров. Электролит, содержащийся во внутреннем пространстве зазора, может изменяться под воздействием гидролиза продуктов коррозии.

С целью защиты металлов от щелевой коррозии принято применять несколько методов:
- уплотнение зазоров и щелей;
- электрохимическая защита;
- процесс ингибирования.
В качестве профилактических методов следует использовать только те материалы, которые в наименьшей степени подвержены возникновению ржавчины, а также изначально грамотно и рационально конструировать газопроводы и другие важные объекты.
Грамотная профилактика во многих случаях представляет собой более простой процесс, чем последующая очистка металлоконструкций от въевшейся ржавчины.
Как проявляется коррозия разных видов
В качестве примера протекания коррозийного процесса можно привести разрушение различных приборов, компонентов автомобилей, а также любых конструкций, произведенных из металла и расположенных:
- в атмосферном воздухе;
- в водах – моря, реки, содержащиеся в почве и под слоями грунта;
- в технических средах и т.д.

В процессе ржавления металл становится многоэлектронным гальваническим элементом. Так, например, если в электролитической среде происходит контакт меди и железа, медь является катодом, а железо – анодом. Отдавая электроны меди, железо в виде ионов попадает в раствор. Ионы водорода начинают двигаться по направлению к меди и там разряжаются. Становясь все более и более отрицательным, катод вскоре приравнивается к потенциалу анода, в результате чего коррозийный процесс начинает замедляться.
Разные виды коррозии проявляются по-разному. Более интенсивно электрохимическая коррозия проявляется в тех случаях, когда в катоде присутствуют вкрапления металла с меньшей активностью по сравнению с корродирующим – на них ржавчина появляется быстрее и является довольно выразительной.
Протекание атмосферной коррозии происходит в условиях влажного воздуха и обычной температуры. В данном случае на поверхности металла образуется пленочка из влаги с растворенным кислородом. Процесс разрушения металла становится интенсивнее по мере увеличения влажности воздуха и содержания газообразных оксидов углерода и серы при условии наличия:
- трещин;
- шероховатостей;
- других факторов, провоцирующих облегчения процесса конденсации.

Почвенная коррозия в наибольшей степени поражает разнообразные подземные сооружения, газопроводы, кабели и другие конструкции. Разрушение меди и других металлов происходит по причине их тесного соприкосновения с почвенной влагой, в составе которой также присутствует растворенный кислород. Разрушение трубопроводов может произойти уже спустя полгода с момента их строительства в том случае, если для почвы, в которой они установлены, характерна повышенная кислотность.
Под воздействием блуждающих токов, исходящих от посторонних объектов, возникает электрическая коррозия. Ее главными источниками являются электрические железные дороги, линии электропередач, а также специальные установки, функционирующие на постоянном электротоке. В большей степени данный вид коррозии провоцирует разрушение:
- газопроводов;
- всевозможных сооружений (мосты, ангары);
- электрокабелей;
- нефтепроводов.
Действие тока провоцирует возникновение участков входа и выхода электронов – то есть, катодов и анодов. Наиболее интенсивным разрушительный процесс является именно на участках с анодами, поэтому на них ржавчина более заметна.
Коррозия отдельных компонентов газопроводов и водяных трубопроводов может быть вызвана тем, что процесс их инсталляции является смешанным, то есть, происходит с использованием различных материалов. Наиболее частыми примерами является точечная коррозия, возникающая в элементах из меди, а также коррозия биметаллов.
При смешанной установке железных элементов со сплавами меди и цинка, процесс коррозии отличается меньшей степенью критичности, чем при медном литье, то есть со сплавами меди, цинка и олова. Предотвратить коррозию трубопроводов можно, используя специальные методы.

Способы защиты от ржавления
Для борьбы с коварной ржавчиной применяются различные методы. Рассмотрим те из них, который являются наиболее эффективными.
Способ №1
Один из самых популярных методов – это электрохимическая защита чугуна, стали, титана, меди и других металлов. На чем же она основывается?
Электрохимическая обработка металлов представляет собой особый способ, направленный на изменение формы, размеров и шероховатости поверхности путем анодного растворения в электролите под воздействием электротока.
Чтобы обеспечить надежную защиту от ржавчины, необходимо еще перед началом эксплуатации металлических изделий обрабатывать их особым средствами, которые в своем составе содержат различные компоненты органического и неорганического происхождения. Данный метод позволяет предотвратить появление ржавчины на определенное время, однако позже придется обновлять покрытие.
 Схема катодной защиты трубопроводов
Схема катодной защиты трубопроводов
Электрозащита представляет собой процесс, при котором металлическая конструкция подключается к внешнему источнику постоянного электрического тока. В результате этого на ее поверхности формируется поляризация электродов катодного типа, и все анодные области начинают преобразовываться в катодные.
Электрохимическая обработка металлов может происходить с участием анода или катода. В некоторых случаях происходит попеременная обработка металлического изделия обоими электродами.
Катодная защита от коррозии необходима в тех ситуациях, когда у металла, подлежащего защите, не наблюдается предрасположенность к пассивации. К металлическому изделию подключается источник внешнего тока – специальная станция катодной защиты. Данный метод подходит для защиты газопроводов, а также трубопроводов водоснабжения и отопления. Однако есть у этого метода определенные недостатки в виде растрескивания и разрушения защитных покрытий – это происходит в случаях значительного смещения потенциала объекта в отрицательную сторону.
Способ №2
Электроискровая обработка металлов может осуществляться при помощи установок различных типов – бесконтактной, контактной, а также анодно-механической.
Способ №3
Для надежной защиты газопроводов и других трубопроводов от ржавчины часто применяется такой метод, как электродуговое напыление. Преимущества данного способа очевидны:

- значительная толщина защитного слоя;
- высокий уровень производительности и надежности;
- применение относительно недорогого оборудования;
- несложный технологический процесс;
- возможность применения автоматизированных линий;
- невысокие энергетические затраты.
Среди недостатков данного метода – невысокая эффективность при обработке конструкций в коррозийных средах, а также недостаточная прочность сцепления со стальной основой в некоторых случаях. В любых других ситуациях такая электрозащита очень эффективна.
Способ №4
Для защиты разнообразных металлических конструкций – газопроводов, мостовых сооружений, всевозможных трубопроводов – требуется эффективная антикоррозийная обработка.

Данная процедура осуществляется в несколько этапов:
- тщательное удаление жировых отложений и масел с применением эффективных растворителей;
- очистка обрабатываемой поверхности от солей, растворимых в воде, – выполняется при помощи профессиональных аппаратов высокого давления;
- удаление имеющихся конструкционных погрешностей, выравнивание кромок – это необходимо для предотвращения сколов наносимого лакокрасочного покрытия;
- тщательная очистка поверхности при помощи пескоструйного аппарата – это делается не только для удаления ржавчины, но и для придания нужной степени шероховатости;
- нанесение противокоррозийного материала и дополнительного защитного слоя.
Правильная предварительная обработка газопроводов и всевозможных металлоконструкций обеспечит им надежную защиту от электрохимической коррозии в процессе эксплуатации.
Причины электрохимической коррозии и способы защиты металла
Электрохимическая коррозия металлов – одна из насущных проблем человечества с того момента, как в производстве различных, необходимых человеку предметов, стали использоваться изделия из металла. Проблема защиты металлов от коррозии всегда стояла остро, потому что под действием разрушительных процессов окисления предметы теряли функциональность, деформировались и приходили в негодность, и нужно было искать способы их защиты.
Когда химия выделилась в отдельную науку, а использование металлов стало приобретать широкое промышленное значение, человечество начало исследовать эти процессы и искать способы борьбы с разрушениями от внешних воздействий.
Что такое коррозия
Процесс разрушения верхнего слоя металлического материала под влиянием внешних воздействий называется коррозией в широком смысле.

Термин коррозия в данном случае – только характеристика того, что металлическая поверхность вступает в химическую реакцию и теряет под её влиянием свои изначальные свойства.
4 основных признака, по которым можно определить, что этот процесс существует:
- процесс, развивающийся на поверхности, и со временем проникающий внутрь металлического изделия;
- реакция возникает самопроизвольно от того, что нарушается устойчивость термодинамического баланса между окружающей средой и системой атомов в сплаве или монолите;
- химия воспринимает этот процесс не просто, как реакцию разрушения, но как реакцию восстановления и окисления: при вступлении в реакцию одни атомы замещают другие;
- свойства и особенности метала при такой реакции претерпевают значительные изменения, или утрачиваются там, где она происходит.
Виды коррозии
В зависимости от типа металла и окислительно-восстановительной реакции, происходящей с ним, коррозия может быть:
- равномерной или неравномерной;
- местной и точечной (отдельные участки почему-либо вступили в реакцию, а другие – нет);
- язвенной, известной еще как питтинг;
- подповерхностной;
- растрескивающейся;
- межкристаллической, возникающая вдоль границ кристалла металла.
Также в зависимости от того, какие именно внешние факторы воздействуют на поверхность, коррозия бывает химической и электрохимической. Химическая коррозия происходит в результате некоторых реакций под влиянием химических взаимодействий, но без участия электрического тока, и может быть присуща даже нефти и газу. Электрохимическая отличается определенными процессами, она более сложная, чем химическая.

На видео: коррозия металлов.
Причины и признаки электрохимической коррозии
Электрохимическая коррозия отличается от химической тем, что процесс разрушения проходит в системе электролитов, отчего внутри этой системы возникает электрический ток. Два сопряжённых процесса, анодный и катодный, приводят к удалению из кристаллической решетки металла неустойчивых атомов. Ионы при анодном переходят в раствор, а электроны от анодного процесса попадают в ловушку к веществу-окислителю и связываются деполяризатором.
Таким образом, деполяризация – это отвод с катодных участков свободных электронов, а деполяризатор – вещество, которое отвечает за этот процесс. Основные реакции происходят с участием водорода и кислорода в роли деполяризаторов.

Существует множество примеров электрохимической коррозии разного типа, которая оказывает воздействие на металлические поверхности в природе и проходит под влиянием различных условий. Водород при этом работает в кислой среде, а кислород – в нейтральной.
Практически все металлы подвергаются электрохимической коррозии, и по этому признаку их разбивают на 4 группы, определяют величину их электродного потенциала:
- активные коррозируют даже в той среде, где нет окислителей;
- среднеактивные вступают в реакцию окисления в кислотной среде;
- малоактивные не вступают в реакцию при отсутствии окислителей и в нейтральных, и в кислых средах;
- не вступают в реакцию — высокой стабильности (благородные металлы, палладий, золото, платина, иридий).
Самый распространенный вид электрохимической коррозии – атмосферная.

Но эта же реакция может протекать и в воде, в растворах оснований, солей и кислот. В узкоспециальном различии атмосферной коррозии различают почвенную и аэрационную, морскую и биологическую (протекающую под воздействием бактерий).
Есть даже электрическая коррозия, которая протекает под воздействием электрического тока, и является результатом работы блуждающих токов, возникающих там, где электрический ток используется человеком для осуществления определенной деятельности.
Гомогенная металлическая поверхность при этом разрушается из-за термодинамической неустойчивости к окружающей среде. А гетерогенная – из-за состава кристаллической решётки, в которой атомы одного металла держатся плотнее, чем атомы инородных вкраплений. Эти реакции отличаются скоростью протекания ионизации ионов, и восстановления окислительных компонентов окружающей среды.
Разрушение металлических поверхностей при электрохимической коррозии состоит в одновременном протекании двух процессов: анодного и катодного, и отличия процессов состоят в том, что растворение происходит на анодах, которые и контактируют с окружающей средой через множество микроэлектродов, которые входят в состав поверхности любого металла и замкнуты на себя.
Характерными примерами электрохимической коррозии можно считать протекание коррозионных процессов на днищах морских судов или в атмосфере на металлических конструкциях.

Необходимость антикоррозионной защиты
Защита металла от воздействий, которые разрушающе действуют на его поверхность – одна из основных задач, возникающих перед теми людьми, которые работают с механизмами, агрегатами и машинами, морскими судами и строительными процессами.
Любой металл, кроме благородных, в той или иной степени, подвергается воздействию разрушительных процессов.

Чем активнее эксплуатируется устройство или деталь, тем больше шансов у нее подвергнуться разрушительному воздействию и атмосферных условий, жидкостей, с которыми приходится сталкиваться в процессе работы. Над защитой металла от коррозии работают многие отрасли науки и промышленного производства, но основные способы остаются при этом неизменными, и состоят в создании защитных покрытий:
- металлических;
- неметаллических;
- химических.
Неметаллические покрытия создаются с помощью органических и неорганических соединений, их принцип действия достаточно эффективен и отличается от остальных типов защиты. Для создания неметаллической защиты в промышленном и строительном производстве используются лакокрасочные составы, бетон и битум и высокомолекулярные соединения, особенно активно взятые на вооружение в последние годы, когда больших высот достигла химия полимеров.

Химия внесла свой вклад в создание защитных покрытий методами:
- оксидирования (создания защитной пленки на металле с помощью оксидных пленок);
- фосфатирования (фосфатных пленок);
- азотирования (насыщения поверхности стали азотом);
- цементации (соединения с углеродом);
- воронения (соединения с органическими веществами);
- изменения состава металла путем введения в него антикоррозийных добавок);
- модификации окружающей коррозийной среды путем введения ингибиторов, влияющих на нее.
Электрохимическая защита от коррозии – это процесс, обратный электрохимической коррозии. В зависимости от смещения потенциала металла в положительную или отрицательную стороны, различают анодную и катодную защиту. Путем подсоединения к металлическому изделию протектора или источника постоянного тока на металлической поверхности создается катодная поляризация, которая и препятствует разрушению металла через анод.
Электрохимические методы защиты состоят в двух вариантах:
- металлическое покрытие защищено другим металлом, у которого более отрицательный потенциал (то есть, защищающий металл менее устойчив, чем защищаемый), и это называется анодное покрытие;
- покрытие нанесено из менее активного металла, и тогда он является и называется катодным.

Анодная защита от коррозии – это, например, оцинкованное железо. Пока не израсходуется весь цинк с защитного слоя, железо будет в относительной безопасности.
Защита катодным способом – это никелирование или нанесение меди. В этом случае разрушение защитного слоя приводит и к разрушению того слоя, который он защищает. Присоединение протектора для предохранения металлического изделия ничем не отличается от протекания реакции в других случаях. Протектор выступает в роли анода, а то, что находится под его протекторатом, остается в сохранности, используя созданные ему условия.
Способы защиты металла
Электрохимическая коррозия – одно из основных препятствий, которые встречаются на пути человеческой деятельности. Защита от воздействия разрушительных процессов и их протекания на поверхности конструкций и сооружений – одна из перманентных и насущных задач любого промышленного производства, и любой бытовой деятельности человека.

Разработано несколько способов такой защиты, и все они активно применяются в повседневном цикле жизнедеятельности:
- Электрохимическая защита – электролитическое по принципу работы использование химических закономерностей, защищает металл с помощью анодного, катодного и протекторного принципа.
- Э лектроискровая обработка с использованием различных установок – бесконтактных, контактных, анодно-механических.
- Электродуговое напыление – основное преимущество в толщине наносимого слоя и относительной дешевизне производимого процесса.
- Эффективная антикоррозийная обработка – удаление загрязнений и очистка обрабатываемой поверхности, с последующим нанесением на поверхность сначала противокоррозионного, а затем и дополнительного защитного слоя.
Все эти способы наработаны в процессе деятельности человека с целью защиты инструментария, средств передвижения и транспортировки на стыке нескольких промышленных отраслей, и с использованием научных достижений.
Электрохимическая коррозия, которая является естественным процессом разрушения поверхности металла под воздействием нейтральных или агрессивных факторов окружающей среды, представляет собой сложную проблему. Убытки от нее терпят и машиностроительные, и транспортные, и промышленные предприятия, средства передвижения. И это проблема, которая требует ежедневного разрешения.
Подробнее о коррозии и ее процессах (1 видео)
Электрохимическая коррозия
Электрохимическая коррозия – самый распространенный вид коррозии. Электрохимическая коррозия возникает при контакте металла с окружающей электролитически проводящей средой. При этом восстановление окислительного компонента коррозионной среды протекает не одновременно с ионизацией атомов металла и от электродного потенциала металла зависят их скорости. Первопричиной электрохимической коррозии является термодинамическая неустойчивость металлов в окружающих их средах. Ржавление трубопровода, обивки днища морского суда, различных металлоконструкций в атмосфере – это, и многое другое, примеры электрохимической коррозии.
К электрохимической коррозии относятся такие виды местных разрушений, как питтинги, межкристаллитная коррозия, щелевая. Кроме того процессы электрохимической коррозии происходят в грунте, атмосфере, море.
Механизм электрохимической коррозии может протекать по двум вариантам:
1) Гомогенный механизм электрохимической коррозии:
– поверхностный слой мет. рассматривается как гомогенный и однородный;
– причиной растворения металла является термодинамическая возможность протекания катодного или же анодного актов;
– К и А участки мигрируют по поверхности во времени;
– скорость протекания электрохимической коррозии зависит от кинетического фактора (времени);
– однородную поверхность можно рассматривать как предельный случай, который может быть реализован и в жидких металлах.
2) Гетерогенный механизм электрохимической коррозии:
– у твердых металлов поверхность негомогенная, т.к. разные атомы занимают в сплаве различные положения в кристаллической решетке;
– гетерогенность наблюдается при наличии в сплаве инородных включений.
Электрохимическая коррозия имеет некоторые особенности: делится на два одновременно протекающих процесса (катодный и анодный), которые кинетически зависимы друг от друга; на некоторых участках поверхности электрохимическая коррозия может принять локальный характер; растворение основного мет. происходит именно на анодах.
Поверхность любого металла состоит из множества короткозамкнутых через сам металл микроэлектродов. Контактируя с коррозионной средой образующиеся гальванические элементы способствуют электрохимическому его разрушению.
Причины возникновения местных гальванических элементов могут быть самые разные:
1) неоднородность сплава
– неоднородность мет. фазы, обусловленная неоднородностью сплава и наличием микро- и макровключений;
– неравномерность окисных пленок на поверхности за счет наличия макро- и микропор, а также неравномерного образования вторичных продуктов коррозии;
– наличие на поверхности границ зерен кристаллов, выхода дислокации на поверхность, анизотропность кристаллов.
2) неоднородность среды
– область с ограниченным доступом окислителя будет анодом по отношению к области со свободным доступом, что ускоряет электрохимическую коррозию.
3) неоднородность физических условий
– облучение (облученный участок – анод);
– воздействие внешних токов (место входа блуждающего тока – катод, место выхода – анод);
– температура (по отношению к холодным участкам, нагретые являются анодами) и т. д.
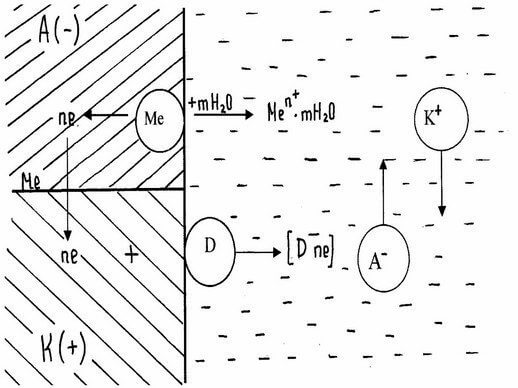
При работе гальванического элемента одновременно протекает два электродных процесса:
Анодный – ионы металла переходят в раствор
Происходит реакция окисления.
Катодный – избыточные электроны ассимилируются молекулами или атомами электролита, которые при этом восстанавливаются. На катоде проходит реакция восстановления.
O2 + 2H2O + 4e → 4OH – (кислородная деполяризация в нейтральных, щелочных средах)
O2 + 4H + + 4e → 2H2O (кислородная деполяризация в кислых средах)
2 H + + 2e → H2 (при водородной деполяризации).
Торможение анодного процесса приводит к торможению и катодного.
При соприкосновении двух электропроводящих фаз (например, мет. – среда), когда одна из них заряжена положительно, а другая отрицательно, между ними возникает разность потенциала. Это явление связано с возникновением двойного электрического слоя (ДЭС). Заряженные частицы располагаются несимметрично на границе раздела фаз.
Скачек потенциалов в процессе электрохимической коррозии может происходить из-за двух причин:
При достаточно большой энергии гидратации ионы металла могут отрываться и переходить в раствор, оставляя на поверхности эквивалентное число электронов, которые определяют ее отрицательный заряд. Отрицательно заряженная поверхность притягивает к себе катионы мет. из раствора. Так на границе раздела фаз возникает двойной электрический слой.
На поверхности металла разряжаются катионы электролита. Это приводит к тому, что поверхность мет. приобретает положительный заряд, который с анионами раствора образует двойной электрический слой.
Иногда возникает ситуация, когда поверхность не заряжена и, соответственно, отсутствует ДЭС. Потенциал, при котором это явление наблюдается называется потенциалом нулевого заряда (φN). У каждого металла потенциал нулевого заряда свой.
Величина электродных потенциалов оказывает очень большое влияние на характер коррозионного процесса.
Скачок потенциала между двух фаз не может быть измерен, но при помощи компенсационного метода можно измерить электродвижущую силу элемента (ЭДС), который состоит из электрода сравнения (его потенциал условно принят за ноль) и исследуемого электрода. В качестве электрода сравнения берется стандартный водородный электрод. ЭДС гальванического элемента (стандартный водородный электрод и исследуемый элемент) называют электродным потенциалом. Электродами сравнения могут также выступать хлорсеребряный, каломельный, насыщенный медно-сульфатный.
Международной конвенцией в Стокгольме 1953г. решено при записях электрод сравнения всегда ставить слева. При этом ЭДС рассчитывать, как разность потенциалов правого и левого электродов.
Если положительный заряд внутри системы движется слева направо – ЭДС элемента считается положительной, при этом
где F – число Фарадея. Если положительные заряды будут двигаться в противоположном направлении, то уравнение будет иметь вид:
При коррозии в электролитах самыми распространенными и значимыми являются адсорбционные (адсорбция катионов или анионов на границе раздела фаз) и электродные потенциалы (переход катионов из металла в электролит или наоборот).
Электродный потенциал, при котором металл находится в состоянии равновесия с собственными ионами называется равновесный (обратимый). Он зависит от природы металлической фазы, растворителя, температуры электролита, активности ионов мет.
Равновесный потенциал подчиняется уравнению Нернста:
где, E ο – стандартный потенциал мет.; R – молярная газовая постоянная; n – степень окисления иона мет.; Т – температура; F – число Фарадея;αMe n+ – активность ионов мет.
При установленном равновесном потенциале электрохимическая коррозия не наблюдается.
Если по электроду проходит электрический ток – равновесное состояние его нарушается. Потенциал электрода изменяется в зависимости от направления и силы тока. Изменение разности потенц., приводящее к уменьшению силы тока, принято называть поляризацией. Уменьшение поляризуемости электродов называют деполяризацией.
Скорость электрохимической коррозии тем меньше, чем больше поляризация. Поляризация характеризуется величиной перенапряжения.
Поляризация бывает трех типов:
– электрохимическая (при замедлении анодного или катодного процессов);
– концентрационная (наблюдается, когда скорость подхода деполяризатора к поверхности и отвода продуктов коррозии мала);
– фазовая (связана с образованием на поверхности новой фазы).
Электрохимическая коррозия наблюдается также при контакте двух разнородных металлов. В электролите они образуют гальванопару. Более электроотрицательный из них будет анодом. Анод в процессе будет постепенно растворяться. При этом идет замедление или даже полное прекращение электрохимической коррозии на катоде (более электроположительном). Например, при контакте в морской воде дюралюминия с никелем интенсивно растворятся будет именно дюралюминий.
Коррозия металлов и способы защиты от нее
| Коррозия – это процесс разрушения металлов и металлических конструкций под воздействием различных факторов окружающей среды – кислорода, влаги, вредных примесей в воздухе. |
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
| Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
При химической коррозии также возможны процессы:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
Fe –2e = Fe 2+
На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
2H + + 2e → H2
O2 + 2H2O + 4e → 4OH –
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
Анод: Fe –2e → Fe 2+
Катод: 2H + + 2e → H2
Суммарная реакция: Fe + 2H + → H2 + Fe 2+
Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
Анод: Fe –2e → Fe 2+
Катод: O2 + 2H2O + 4e → 4OH –
Суммарная реакция:
Fe 2+ + 2OH – → Fe(OH)2
4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
При этом образуется ржавчина.
Методы защиты от коррозии
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.
Защита от химической и электрохимической коррозии
Электрохимическая коррозия – это самый распространенный вид повреждения, поражающий металлы. Расскажем о методах анодной защиты металлов, отличиях от химической коррозии.

Больше всего металлы боятся коррозии. Она способна привести в негодность самые прочные конструкции. Огромные мосты, линии электропередач, километровые трубопроводы становятся беспомощными перед разрушающим процессом. Чтобы повреждения не допустить, металл защищают. Но важно понимать, что бывает несколько видов окисления. Электрохимическая коррозия, химическая или газовая – все они похожи по следствиям, но эффективными методами защиты от каждого вида будут свои индивидуальные мероприятия, зависящие от многих факторов.
Коррозия электрохимического плана наиболее часто поражает металлы. Это связано с тем, что они, как правило, неустойчивы термодинамически в среде, которая их окружает, а последняя чаще представляет обычный электролит, то есть проводник. Поэтому за счет металла коррозионная среда стремится к восстановлению путем переноса частиц через электрический ток.

Суть, причины и признаки химической коррозии
Для возникновения химической коррозии нужно не так уж много: металл и соответствующая коррозионная среда. Причины большой вероятности появления окисления – это неустойчивое термодинамическое состояние металла и стремление его перейти к более устойчивому состоянию. Словесной формулой это можно выразить следующим образом:
Исходный металл + среда окислительного характера = протеканию реакции = результату в виде ржавчины.
Основной признак химической коррозии – окислительная среда – не является электролитом как при электрохимической, то есть окислительно-восстановительные процессы имеют чисто химический подтекст. Химическая коррозия бывает двух видов:
- та, которая протекает в газовой среде, когда температура вокруг очень высока;
- второй вид химической коррозии связан с жидкостями.
Для идеальной защиты от коррозии необходимо проводить мероприятия комбинированной защиты, так как в реальности на металл воздействует одновременно и электрохимическое, и химическое окисление.
Отличия химической коррозии от электрохимической
Под процессом электрохимической коррозии понимают окислительно-восстановительную реакцию коррозионной среды за счет электронов металла, которые отнимаются у него под воздействием электрического потенциала, возникающего в электролите, коим является эта окислительная среда. Ионизация сопровождается разрушением той части, которая непосредственно контактирует со средой, а ржавчина, видимая невооруженным глазом, не что иное, как восстановленная коррозионная среда.

- Сущностью электрохимической коррозии является процесс, протекающий в электролите, и это главное.
- В электрохимической обязательно присутствует электрический ток, чего нет при химическом окислении.
- Электрохимическая коррозия характеризуется не одномоментным переходом частиц от металла к окислительному компоненту, а определяется величиной потенциала. То есть, чем потенциал выше, тем больше скорость движения частиц и быстрее восстановительный процесс коррозионной среды. При химическом же процессе разрушение вещества сопровождается одновременным восстановлением коррозионной среды.
Выделяют следующие виды электрохимической коррозии:
- Межкристаллитная. Электрохимическое явление, когда у алюминия, никеля, иных элементов наблюдается разрушение зерна по его границе, и происходит это избирательно. В результате конструкция теряет свою прочность, ухудшаются свойства пластичности. Опасность в том, что этот электрохимический процесс визуально может быть незаметен.
- Питтинговая. Проявляется как поражение точечных участков на таких элементах, как медь, ее сплавы и другие. Размер отдельных участков, где проявляется коррозия, обычно не превышает 1.5 миллиметров. Электрохимический питтинг бывает поверхностного типа, а также открытый и закрытый.
- Щелевая. Опасный вид электрохимической коррозии, сопровождающийся быстрым усиленным разрушением областей, где есть микротрещины, зазоры либо щели. Коррозия может протекать при любом состоянии окружающей среды.
Протекторная защита от электрохимической коррозии
Анодную защиту нужно периодически возобновлять, ведь «жертвенный металл» в процессе эксплуатации также очень сильно разрушается, особенно если он не совсем правильно подобран для работы в конкретной среде.
Основные случаи, когда применение протекторной защиты будет оправдано:
- Недостаточно средств на проведение более дорогостоящих защитных мероприятий.
- Если защитой нужно обеспечить конструкции из металла небольших габаритов.
- Когда трубопроводы имеют дополнительную поверхностную изоляцию.
Такую защиту от электрохимической коррозии, как протекторная, применяют, в основном, к разным маркам стали. Здесь уместным будет использование протекторов на основе кадмия, алюминия, магния, хрома, цинка, но используется не чистый элемент, а сплавы.
Цинковые протекторы
- до 0.15% кадмия при минимально возможном процентном соотношении в 0.025%;
- до 0.5% алюминия;
- примеси железа, свинца и меди, общей суммой не превышающие 0.005%.
Наиболее эффективное применение цинка выявлено в морской воде, где с помощью таких протекторов успешно работает защита, например, газовых или нефтяных магистралей. Плюс цинка еще в том, что он допустим к использованию со взрывоопасными веществами. Когда происходит растворение анода, не наблюдается выделения загрязняющих веществ, которые могут навредить экологии.
Применение цинковых протекторов в водоемах, где вода имеет пресный состав либо в грунте под землей сопровождается быстрым образованием на поверхности протектора таких соединений, как оксиды и гидроксиды, которые приводят к торможению электрохимического процесса окисления анода, и фактически прекращается защита основного металла от электрохимической коррозии.
Установка цинкового протектора на днище корабля:

Магниевые протекторы
- максимум 5%, минимум 2% цинка;
- максимум 7%, минимум 5% алюминия;
- небольшое содержание меди, никеля и свинца, не более десятых долей процента.
Протекторы из магния хороши, когда среда, в которой они применяются, имеет pH не выше 10.5, что соответствует грунтам обычного характера, водным объектам со слабосоленой акваторией либо попросту пресной воде. Для защиты подходят любые трубопроводы и металлоконструкции, находящиеся в описанных выше условиях. Применение магния в агрессивных соленых растворах сопровождается быстрым образованием плохо растворимой пленки на его поверхности.
В некоторых случаях магниевые протекторы влияют на металл таким образом, что последний становится более хрупким, и в теле конструкции могут образовываться трещины. Прежде чем применять магний для защиты от электрохимической коррозии конкретной марки стали, нужно провести дополнительные исследования, чтобы избежать негативных последствий.
Алюминиевые протекторы
Целевое назначение протекторов из алюминия – работать в качестве защиты от электрохимической коррозии в средах с водой проточной с соленым составом, например, в прибрежных морских водах. В составе сплава протектора из алюминия имеются:
- примеси индия, кадмия, кремния не более 0.02%;
- цинка – до 8%;
- магния – до 5%.
Благодаря этим дополнительным металлам нет возможности появления на протекторе жесткой, задерживающей растворение пленки. Допустимо применять алюминиевый протектор и в средах, подходящих для магниевого протектора.
Способы защиты металлов от химической коррозии
- Метод конструкционного решения проблемы. Он связан с тем, чтобы использовать сплавы, которые имеют очень высокую устойчивость к коррозии, либо применять биметаллические композиции, где основной конструкционный металл покрыт тонким слоем устойчивого соединения (например, оцинковку).
- Метод улучшения среды, где будет эксплуатироваться изделие, путем изменения pH, нейтрализации агрессивных составляющих коррозионной среды.
- Метод пассивной защиты, наиболее известный тем, что доступ к поверхности конструкции в коррозионной среде блокируется пленкой из неактивного и не вступающего в реакцию материала. Это покрытие разного рода лакокрасочными компонентами для защиты от коррозии.
Если вы сталкивались с электрохимической коррозией, имеете профильное образование, ориентируетесь в вопросах защиты металла, получили практические навыки по организации протекторной защиты металлоконструкций либо применяли метод катодной защиты, поделитесь своими знаниями в комментариях.






